Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã phê duyệt Farxiga (Dapagliflozin) có hiệu quả giảm tỉ lệ nhập viện do suy tim ở người bệnh đái tháo đường type 2 có mắc kèm bệnh lý tim mạch hoặc có nhiều yếu tố nguy cơ mắc bệnh lý tim mạch.

Sự phê duyệt này dựa trên kết quả nghiên cứu DECLARE-TIMI 58, nghiên cứu lớn nhất cho đến hiện nay thực hiện với thuốc ức chế SGLT2. Nghiên cứu này so sánh đánh giá hiệu quả của Farxiga so với giả dược trên biến cố tim mạch ở bệnh nhân đái tháo đường type 2 có nguy cơ gặp những biến cố này, bao gồm bệnh nhân có nhiều yếu tố nguy cơ bệnh tim mạch hoặc đã mắc bệnh tim mạch. Đồng thời nghiên cứu cũng đánh giá tiêu chí phụ về hiệu quả trên thận của thuốc.
Nghiên cứu tiến hành trên 17.000 bệnh nhân, thực hiện tại 882 cơ sở nghiên cứu thuộc 33 quốc gia.
Kết quả cho thấy Farxiga giảm tỉ lệ nhập viện do suy tim hoặc tử vong do biến cố tim mạch so với giả dược là 17%. Tỉ lệ này ổn định với toàn bệnh nhân được nghiên cứu, bao gồm bệnh nhân đã mắc bệnh tim mạch trước đó và bệnh nhân có nhiều yếu tố nguy cơ mắc bệnh tim mạch.
Farxiga (Dapagliflozin) là thuốc gì?
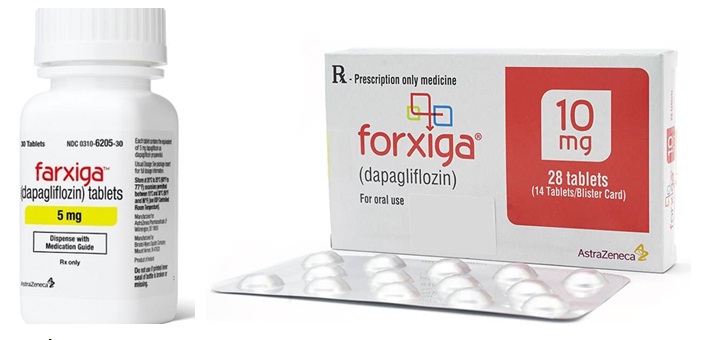
Dapagliflozin là thuốc điều trị đái tháo đường thuộc nhóm ức chế thụ thể SGLT2. Farxiga là tên thương mại được lưu hành tại Mỹ. Tại Việt Nam, loại thuốc điều trị đái tháo đường chứa Dapagliflozin có tên là Forxiga, được Cục quản lý Dược cấp phép lưu hành năm 2015.
Dapagliflozin được chỉ định sử dụng đơn độc hoặc trong phác đồ phối hợp kiểm soát đường huyết, với lợi ích kèm theo là giảm cân và giảm huyết áp khi kết hợp với điều chỉnh chế độ ăn và tập thể dục ở bệnh nhân đái tháo đường type 2. Thuốc không khuyến cáo dùng cho bệnh nhân đái tháo đường type 1 hoặc toan ceton do đái tháo đường.
Cơ chế tác dụng của Dapagliflozin
Cơ chế tác dụng của thuốc là ức chế mạnh, chọn lọc và có phục hồi SGLT2 (Sodium-glucose co-transporter: hệ đồng vận chuyển Natri-glucose) tại thận. Đây là hệ vận chuyển chính phụ trách việc tái hấp thu glucose từ dịch lọc cầu thận về máu tuần hoàn. Dapagliflozin làm giảm glucose máu do ức chế tái hấp thu glucose ở ống thận và tăng bài tiết glucose qua nước tiểu, từ đó giúp giảm glucose máu bất kể tình trạng đề kháng với insulin và khả năng tiết insulin của tuyến tụy.
Đồng thời, dựa trên cơ chế này, thuốc có hiệu quả giảm glucose ở người bệnh tăng glucose lúc đói hoặc tăng glucose sau ăn. Glucose được bài tiết ra nước tiểu ngay sau khi sử dụng liều thuốc đầu tiên, hiệu quả của thuốc duy trì tiếp 24 giờ sau đó và trong suốt quá trình điều trị.
Tác dụng bài tiết glucose qua nước tiểu của Dapagliflozin có liên quan đến sự mất calo và giảm cân. Đồng thời, cơ chế này cũng có thể gây tác dụng lợi tiểu ở người bệnh.
Ai không nên dùng thuốc Farxiga (Dapagliflozin)?
Chống chỉ định:
- Người bệnh có phản ứng quá mẫn nghiêm trọng với thuốc.
- Suy thận nặng, bệnh thận giai đoạn cuối hoặc người bệnh có lọc máu.
Cảnh báo và thận trọng:
- Tụt huyết áp: Do tác dụng lợi tiểu nên thuốc có thể gây giảm thể tích tuần hoàn dẫn đến tình trạng tụt huyết áp.
- Nhiễm toan ceton: Đã có báo cáo về tình trạng toan ceton ở bệnh nhân đái tháo đường type 1 và 2 dùng Dapagliflozin, có một số trường hợp tử vong.
- Tổn thương thận cấp tính: Do tác dụng gây co thắt nội mạch nên thuốc có khả năng gây tổn thương thận cấp tính.
- Viêm đài bể thận và nhiễm khuẩn huyết nguyên nhân từ đường tiết niệu: Các chất ức chế SGLT2 (trong đó có Farxiga) làm tăng nguy cơ mắc bệnh nhiễm khuẩn đường tiết niệu.
- Hạ đường huyết: Farxiga làm tăng nguy cơ hạ đường huyết khi dùng đồng thời với insulin hoặc các chất kích thích bài tiết insulin.
- Nhiễm nấm sinh dục: Farxiga làm tăng nguy cơ viêm bộ phận sinh dục do nấm, đặc biệt ở bệnh nhân đã có tiền sử mắc bệnh.
Tài liệu tham khảo:
1. “Farxiga approved in the US to reduce the risk of hospitalisation for heart failure in patients with type-2 diabetes” AstraZeneca – US published 21 October 2019
2. “Farxiga significantly reduced hospitalisation for heart failure or CV death in a broad patient population with type-2 diabetes in the landmark DECLARE-TIMI 58 trial” AstraZeneca published 12 November 2018
3. SmPC of Forxiga 10 mg film-coated tablets, The electronic medicines compendium (emc), last update 31st July 2019






